Периодический закон
К середине XIX века учёные располагали множеством сведений о физических и химических свойствах разных элементов и их соединений. Появилась необходимость упорядочить эти знания и представить их в наглядном виде. Исследователи из разных стран пытались создать классификацию, объединяя элементы по сходству состава и свойств веществ, которые они образуют. Однако ни одна из предложенных систем не охватывала все известные элементы.
Пытался решить эту задачу и молодой русский профессор Д.И. Менделеев. Он собирал и классифицировал информацию о свойствах элементов и их соединений, а затем уточнял её в ходе многочисленных экспериментов. Собрав данные, Дмитрий Иванович записал сведения о каждом элементе на карточки, раскладывал их на столе и многократно перемещал, пытаясь выстроить логическую систему. Долгие научные изыскания привели его к выводу, что свойства элементов и их соединений изменяются с возрастанием атомной массы, однако не монотонно, а периодически.
Так был открыт периодический закон, который учёный сформулировал следующим образом: «Свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса».
Своё открытие Менделеев совершил почти за 30 лет до того, как учёным удалось понять структуру атома. Открытия в области атомной физики позволили установить, что свойства элементов определяются не атомной массой, а зависят от количества электронов, содержащихся в нём. Поэтому современная формулировка закона звучит так:
Свойства химических элементов, а также формы и свойства образуемых ими веществ и соединений находятся в периодической зависимости от величины зарядов ядер их атомов.
Этот принцип Менделеев проиллюстрировал в таблице, в которой были представлены все 63 известных на тот момент химических элемента. При её создании учёный предпринял ряд весьма смелых шагов.
Во-первых, многочисленные эксперименты позволили Менделееву сделать вывод, что атомные массы некоторых элементов ранее были вычислены неправильно, и он изменил их в соответствии со своей системой.
Во-вторых, в таблице были оставлены места для новых элементов, открытие которых учёный предсказал, подробно описав их свойства.
Первый вариант Периодической таблицы элементов, составленной Д.И. Менделеевым.
Мировое научное сообщество поначалу скептически отнеслось к открытию русского химика. Однако вскоре были открыты предсказанные им химические элементы: галлий, скандий и германий. Это разрушило сомнения в правильности системы Менделеева, которая навсегда изменила науку. Там, где раньше учёному требовалось провести ряд сложнейших (и даже не всегда возможных в реальности) опытов — теперь стало достаточно одного взгляда в таблицу.
Теперь расскажем, как устроена Периодическая таблица элементов Менделеева и как ею пользоваться.
Популярное
|
Началось! Врач Владимир Зеленко обратился в Раввинский Суд по поводу коронавирусного геноцида! 4579 |
|
Статистики судеб вакцинированных и невакцинированных детей 1991 |
|
Новости сталинских репрессий. Явление Богуславского 1455 |
|
Зазнобин Владимир Михайлович. Биография 1452 |
|
«Мир пошёл под нож? 1322 |
|
COVID-19 и Вакцинация — что это? 1299 |
|
Что видят осознанные: В.Багдасарян, Д.Перетолчин, С.Грошев, В.Ефимов, Нестор, Е.Именитов М.Ковальчук 1298 |
|
Не проспать Восход: Атака разумных от народа 1178 |
|
Алгоритмика мышления. Цитатно-догматическое богословие как формирующий фактор ошибок 1140 |
|
Наша колея в Афганистане 1131 |
|
Надо ли жалеть Авериных? 1118 |
|
Сир, вы будете принимать ликование России ? 1033 |
|
Почему столицу переносят в Сибирь? 1030 |
|
Как мы до такого докатились 996 |
|
Страна обломовых 967 |
|
За кем придут из министерства правды? 948 |
|
Воплощение второго смыслового ряда сказки Пушкина 929 |
|
Бегущие янки и демократия у нас 921 |
|
МЁД, или как капитализм ест сам себя. 903 |
|
Кто внушает русофобию Европе. Пламен Пасков 842 |
|
Зазнобинские чтения 2-5 сентября 2021 823 |
|
Денежная радиация и Русский Дух 816 |
Группы элементов с похожими свойствами
Группа — это вертикальная колонка в периодической таблице, определяющая основные физико-химические свойства элементов. Вещества, принадлежащие к одной и той же группе, обладают похожими химическими особенностями и демонстрируют одинаковую закономерность в изменении своих свойств по мере увеличения атомного числа.
Всем группам (колонкам таблицы) присваиваются номера от 1 до 18 — слева направо (от щелочных металлов к благородным газам). Такая система вступила в силу в 1988 году по инициативе ИЮПАК. Все прежние названия групп, которые использовали в разных странах, больше не употребляются.
Элементы, которые относятся к одной группе, показывают следующие закономерности по направлению сверху вниз:
- Возрастает радиус атома элементов в рамках одной группы.
- Усиливаются металлические свойства элементов и ослабевают неметаллические.
- Падает электроотрицательность.
Цветовое определение групп
Вещества в каждой группе делятся на те, которые находятся в главной подгруппе и те, которые входят в побочную подгруппу. В таблице составляющие побочной группы выделяются синим цветом, к ней относятся элементы только больших периодов (начинаются с четвертого периода). В главную подгруппу могут входить элементы и малых, и больших периодов (начинаются с первого или второго периодов).
Цезий как эталон самого точного времени в мире
Цезий – прекрасный пример управляемого хаоса. Этот элемент известен как радиоактивный отход от ядерных взрывов. Цезий является одним из пяти элементов, которые находятся в жидком состоянии при комнатной температуре.
Но самое удивительное изменение состояния цезия происходит, когда вы помещаете его в воду. Вот что при этом происходит:
Также у цезия электронные переходы настолько точны, что он стал использоваться в качестве основного стандарта для определения самого точного в мире времени.
Так, секунда – это время, равное 9 192 631 770 периодам излучения, соответствующего переходу между двумя сверхтонкими уровнями основного состояния атома цезия-133.
Цезий применяется в атомных часах. Вот как они выглядят:
hodinkee.com
Эти атомные часы настолько точны, что не потеряют ни секунды за 20 миллионов лет. Это безумие, как такой нестабильный элемент может быть использован, чтобы стать нашим точным определением времени.
История добычи серебра с древних времен: разное значение и применение
Условный срок знакомства человека с серебром измеряется 6 тысячелетиями. Такой возраст имеют самые древние украшения, обнаруженные при раскопках на Ближнем Востоке. Во времена Вавилона и Ассирии металл считался магическим элементом Луны, имеющим мистическое значение. Эту роль он выполнял также во времена Средневековья: алхимики рассматривали необычного цвета вещество как второй по совершенству металл и неотъемлемую часть Великого Делания.
Ковкость, красота, относительная устойчивость к окислению обеспечили металлу еще одно применение. Для первых на свете денег в виде монет использовался сплав золота или серебра.
Коэффициент соотношения цены благородных металлов, введенный И. Ньютоном, сыграл в популяризации серебра немаловажную роль.
 AG серебро химический элемент
AG серебро химический элемент
В 13 веке появилась серебряная посуда и подсвечники, позже – приборы, инструменты. С 19 века, когда человечество освоило электричество, металл, его сплавы стали незаменимыми для изготовления электротехники.
Достойное
- неделя
- месяц
- год
- век
|
Мы знаем, где мозги у Эрдогана |
|
Нас мало, но КПД за 100 процентов! |
|
Эмиссия рисков – триллер с участием финансовых корпораций |
|
Мы знаем, где мозги у Эрдогана |
|
Страна обломовых |
|
«Балансирование, поддерживающее стабилизец» |
|
Наша колея в Афганистане |
|
Денежная радиация и Русский Дух |
|
Чьё оно – Овертоново окно? |
|
Парус судьбы: От боли душевной в резонанс сердец! |
|
Методологическая философия. Предельно обобщающие понятия. Триединство |
|
Главный итог уходящего года |
|
Маски и перчатки убивают |
|
Памяти великого человека Земли Русской Владимира Михайловича Зазнобина |
|
Путеводные заметки: Свет Лей |
|
Контакт с «тонким миром» |
|
Свинство матрицы «успешности» и молодёжь |
|
Точка невозврата и клинический разврат |
|
Зазнобин Владимир Михайлович. Биография |
|
Чисто чтобы не забыть, первыми в космос вышли русские |
|
Центральный банк России работает на её уничтожение |
|
Ну, за самодержание!… |
|
7 советов от гениального врача Николая Амосова . |
|
Белые ночи почтальона Алексея Тряпицына: отчёт «победителям»? |
|
Другой взгляд на пенсионный вопрос или какое государство нам нужно |
|
Самые яркие примеры смекалки у советских солдат |
|
Смотрите ж: всё стоит она! |
Организация периодической системы
Химические элементы в таблице Д. И. Менделеева расположены по рядам, в соответствии с возрастанием их массы, а длина рядов подобрана так, чтобы находящиеся в них элементы имели схожие свойства. Например, благородные газы, такие как радон, ксенон, криптон, аргон, неон и гелий с трудом вступают в реакции с другими элементами, а также имеют низкую химическую активность, из-за чего расположены в крайнем правом столбце. А элементы левого столбца (калий, натрий, литий и т.д.) отлично реагируют с прочими элементами, а сами реакции носят взрывной характер. Говоря проще, внутри каждого столбца элементы имеют подобные свойства, варьирующиеся при переходе от одного столбца к другому. Все элементы, вплоть до №92 встречаются в природе, а с №93 начинаются искусственные элементы, которые могут быть созданы лишь в лабораторных условиях.
В своём первоначальном варианте периодическая система понималась только как отражение существующего в природе порядка, и никаких объяснений, почему всё должно обстоять именно так, не было. И лишь когда появилась квантовая механика, истинный смысл порядка элементов в таблице стал понятен.
Химические характеристики элемента
Химические свойства не слишком разнообразны: вещество достаточно инертно, как благородный металл не растворяется соляной или серной кислотой. Но если создать определенные условия, металл проявит химическую активность.
| Реагент | Реакция |
|---|---|
| O2 | С кислородом воздуха не взаимодействует даже при высоких температурах . Возможно получение оксида при взаимодействии с озоном |
| H2S + O2 | Образует соединение с серой, при наличии даже ее следов |
| Галогены (CL2, I2) | Окисляют до галогенида |
| S | Реакция идет при нагревании до сульфида |
| FeCl3 | Растворяется, образуя хлорид |
| HNO3 | Взаимодействует с горячей концентрированной кислотой |
 Серебро в пробирке
Серебро в пробирке
Электронная периодическая таблица Д.И.Менделеева
В данной таблице обозначены группы элементов, периоды и ряды. Элементы в таблице цветные, где розовый – s-элементы; желтый – p-элементы; синий – d-элементы; зеленые – f-элементы.
* Чтобы узнать описание элемента, нажмите на него. Оранжевой рамкой выделены неметаллы.
| пери-оды | ряды | группы элементов | |||||||||||||
| I | II | III | IV | V | VI | VII | VIII | ||||||||
| a | b | a | b | a | b | a | b | a | b | a | b | a | b | b | a |
| 1 | 1 | ||||||||||||||
| 2 | 2 | ||||||||||||||
| 3 | 3 | ||||||||||||||
| 4 | 4 | ||||||||||||||
| 5 | |||||||||||||||
| 5 | 6 | ||||||||||||||
| 7 | |||||||||||||||
| 6 | 8 | ||||||||||||||
| 9 | |||||||||||||||
| 7 | 10 | ||||||||||||||
| высшие оксиды | |||||||||||||||
| летучие водородные соединения | |||||||||||||||
| лантаноиды | |||||||||||||||
| актиноиды | |||||||||||||||
Периодическая таблица Д.И. Менделеева:
Периодическая таблица Дмитрия Ивановича Менделеева является графическим представлением закона, описывающего повторяющееся изменение совокупности свойств химических элементов в зависимости от заряда ядер их атомов (говоря иначе – от конфигураций атомных электронных оболочек), открытого учёным в 1869 году.
Изначальный вариант таблицы демонстрировал периодичность изменений свойств с ростом атомного веса (атомной массы) химических элементов. К настоящему моменту существует уже несколько сотен вариантов графического представления этого периодического закона, причём каждый из них подчёркивает специфическую схему периодичности изменения выбранных свойств элементов.
Внутренняя структура:
Наиболее часто таблица Дмитрия Ивановича Менделеева изображается в двумерном варианте, где каждый вертикальный столбец (его принято называть группой) определяет все основные физико-химические свойства включённых в него элементов. Горизонтальные же строки образуют т.н. периоды, внутри которых при взаимном сравнении также прослеживается подобие в изменении свойств включённых в строку-период элементов: открывается период типичным металлом, а заканчивается благородным газом через предшествующую ему череду элементов со всё более и более неметаллическими свойствами.
Согласно современным теориям строения атома (как самого ядра, так и его электронных оболочек), таблица Дмитрия Ивановича Менделеева демонстрирует периодичность свойств элементов, диктуемую последовательным (от низших к высшим) заполнением электронных оболочек атома. Тип и энергетическая последовательность этих оболочек определяются квантовомеханическими расчётами, а совокупность распределения всех электронов атома описывается т.н. электронной конфигурацией – формулой, где указывается фактическое нахождение электронов на электронных оболочках атома химического элемента. Обычно только находящиеся на самых внешних (валентных) оболочках электроны участвуют в установлении связей между атомами, что определяет проявляющиеся химические свойства конкретного элемента.
Различают следующие свойства химических элементов: металличность и неметалличность.
Металличность – способность отдавать свои электроны (характеризуется через потенциал ионизации и растёт в группе элементов периодической таблицы сверху вниз, а в периодах – справа налево).
Неметалличность – способность принимать чужие электроны (описывается через энергию сродства к электрону, возрастает в группе таблицы снизу вверх, а в периодах – слева направо).
Примечание: @ Видео https://www.youtube.com/watch?v=QJfuCZvqhRM
Структура таблицы
В таблице Менделеева химические вещества расположены в специальном порядке: слева направо по мере роста их атомных масс. Все они в периодической системе объединены в периоды и группы. Таблица состоит из семи периодов и восьми групп.
Периоды — это горизонтальные ряды в таблице.
Элементы, которые относятся к одному периоду, показывают следующие закономерности с увеличением их порядкового номера:
- Возрастает электроотрицательность.
- Металлические свойства убывают, неметаллические возрастают.
- Атомный радиус падает.
Периоды в таблице делятся на:
- малые;
- большие.
Малыми называются периоды, которые содержат небольшое количество элементов. Это первый, второй и третий периоды, первый состоит из 2-х, второй и третий из 8 элементов.
Все остальные периоды — это большие периоды. Четвертый и пятый состоят из 18 элементов, шестой — из 32-х, седьмой — из 24-х.
В нижней части таблицы Менделеева расположены химические вещества, которые называются лантаноидами и актиноидами.
Таблица периодической системы содержит десять рядов. Малые периоды состоят из одного ряда, большие периоды содержат по два ряда. В седьмом периоде находится один ряд.
Каждый большой период состоит из четного и нечетного рядов. В четных рядах содержатся металлы, в нечетных рядах — неметаллы.
Периодическая система начинается водородом — первым химическим элементом, а заканчивается на сегодняшний день 118-м — оганесоном. Ученые утверждают, что таблица не закончена, идет активный поиск 119-го элемента.
Группы
Вертикальные столбики элементов в периодической таблице — группы состоят из подгрупп: главной и побочной, они иногда обозначаются буквами А и Б соответственно.
В состав главных подгрупп входят s- и р-элементы, а в состав побочных — d- и f-элементы больших периодов.
Главная подгруппа — это совокупность элементов, которая размещается в периодической таблице вертикально и имеет одинаковую конфигурацию внешнего электронного слоя в атомах.
Как следует из приведенного определения, положения элемента в главной подгруппе определяется общим количеством электронов (s- и р-) внешнего энергетического уровня, равным номеру группы. Например, сера (S — 3s2 3p4 ), в атоме которого на внешнем уровне содержится шесть электронов, относится к главной подгруппе шестой группы, аргон (Ar — 3s2 3p6 ) — к главной подгруппе восьмой группы, а стронций (Sr — 5s2 ) — к ІІА-подгруппе.
Элементы одной подгруппы характеризуются сходством химических свойств. В качестве примера рассмотрим элементы ІА и VІІА подгрупп (табл.2). С ростом заряда ядра увеличивается количество электронных слоев и радиус атома, но количество электронов на внешнем энергетическом уровне остается постоянной: для щелочных металлов (подгруппа IА) — один, а для галогенов (подгруппа VIIА) — семь. Поскольку именно внешние электроны наиболее существенно влияют на химические свойства, то понятно, что каждая из рассмотренных групп элементов-аналогов имеет подобные свойства.
Но в пределах одной подгруппы наряду с подобием свойств наблюдается их некоторое изменение. Так, элементы подгруппы ІА все, кроме Н — активные металлы. Но с ростом радиуса атома и количества электронных слоев экранирующих влияние ядра на валентные электроны, металлические свойства усиливаются. Поэтому Fr более активный металл, чем Сs, a Cs — более активный, чем R в и т.д. А в подгруппе VIIA по той же причине ослабляются неметаллические свойства элементов при росте порядкового номера. Поэтому F — более активный неметалл по сравнению с Cl, a Cl — более активный неметалл сравнению с Br и т.д.
Таблица 2 — Некоторые характеристики элементов ІА и VІІА-подгрупп
| период | Подгруппа IA | Подгруппа VIIA | ||||||
|---|---|---|---|---|---|---|---|---|
| Символ элемента | Заряд ядра | Радиус атома, нм | Внешняя электронная конфигурацiя | Символ элемента | Заряд ядра | Радиус атома, нм | Внешняя электронная конфигурацiя | |
| II | Li | +3 | 0,155 | 2 s 1 | F | +9 | 0,064 | 2 s 2 2 p 5 |
| III | Na | +11 | 0,189 | 3 s 1 | Cl | +17 | 0,099 | 3 s 2 3 p 5 |
| IV | K | +19 | 0,236 | 4 s 1 | Br | 35 | 0,114 | 4 s 2 4 p 5 |
| V | Rb | +37 | 0,248 | 5 s 1 | I | +53 | 0,133 | 5 s 2 5 p 5 |
| VI | Cs | 55 | 0,268 | 6 s 1 | At | 85 | 0,140 | 6 s 2 6 p 5 |
| VII | Fr | +87 | 0,280 | 7 s 1 | — | — | — | — |
Побочные подгруппа — это совокупность элементов, размещаемых в периодической таблице вертикально и имеют одинаковое количество валентных электронов за счет застройки внешнего s- и втором снаружи d-энергетических подуровней.
Все элементы побочных подгрупп относятся к d-семейству. Эти элементы иногда называют переходными металлами. В побочных подгруппах свойства изменяются более медленно, поскольку в атомах d-элементов электроны застраивают второй извне энергетический уровень, а на внешнем уровне находятся только один или два электрона.
Положение первых пяти d-элементов (подгруппы IIIБ- VIIБ) каждого периода можно определить с помощью суммы внешних s-электронов и d-электронов второго снаружи уровня. Например, из электронной формулы скандия (Sc — 4s2 3d1 ) видно, что он размещается в побочной подгруппе (поскольку является d-элементом) третьей группы (поскольку сумма валентных электронов равна трем), а марганец (Mn — 4s2 3d5 ) размещается в побочной подгруппе седьмой группы.
Положение последних двух элементов каждого периода (подгруппы IБ и IIБ) можно определить по количеству электронов на внешнем уровне, поскольку в атомах этих элементов предыдущий уровень является полностью завершенным. Например, Ag ( 5s1 5d10 ) размещается в побочной подгруппе первой группы, Zn ( 4s2 3d10 ) — в побочной подгруппе второй группы.
Триады Fe-Co-Ni, Ru-Rh-Pd и Os-Ir-Pt размещены в побочной подгруппе восьмой группы. Эти триады образуют две семьи: железа и платиноидов. Кроме указанных семей отдельно выделяют семью лантаноидов (четырнадцать 4f-элементов) и семью актиноидов (четырнадцать 5f-элементов). Эти семьи принадлежат к побочной подгруппе третьей группы.
Рост металлических свойств элементов в подгруппах сверху вниз, а также уменьшение этих свойств в пределах одного периода слева направо обусловливают появление в периодической системе диагональной закономерности. Так, Be очень похож на Al, B — на Si, Ti — на Nb. Это ярко проявляется в том, что в природе эти элементы образуют подобные минералы. Например, в природе Те всегда бывает с Nb, образуя минералы — титанониобаты.
Многомерное химическое пространство
Бинарные соединения легко визуализировать: их химическое пространство — это просто плоский лист бумаги. А тройные соединения — это уже куб. Четвертные соединения визуализировать никак не получится, разве что в проекции. Но вы можете создать алгоритм, который будет справляться с соединениями любой химической сложности, ведь для компьютера любое четырехмерное или даже двадцатимерное пространство совершенно не проблема.
Кстати, даже в бинарном пространстве эта проблема совершенно нетривиальная и очень-очень сложная. Там будет 2000 бинарных систем, и в каждой можно придумать огромное число соединений. Какие-то из них будут стабильными, какие-то нет, и заранее не всегда понятно какие. Для каждого соединения можно придумать астрономическое множество кристаллических структур, а это тоже будет определять свойства.
Если мы повышаем химическую сложность и идем к тройным-четверным системам, то там становится чудовищно сложно. Сами посудите, сколько известно соединений четырех элементов. Углерод, водород, азот, кислород — вся органика, бессчетное множество! Мы используем менделеевские числа только для визуализации: когда нужно построить химическое пространство для бинарных или тройных соединений и мы хотим увидеть, где именно живут хорошие соединения. Но на самом деле компьютеру проще и лучше справляться с более сложным пространством.
Таблица Менделеева важна, но Периодический закон – ещё важнее
 Менделеев смог открыть один из всеобъемлющих законов
Менделеев смог открыть один из всеобъемлющих законов
Как ни странно, важнейшее открытие Менделеева обычно остается за кадром – Периодический закон:
Современная формулировка практически ничего не меняет, лишь дополняя исходный текст:
Периодическая система стала графическим выражением Периодического закона, который устанавливает зависимость свойств элементов от их атомного веса (атомной массы или атомного числа — числа протонов в атоме).
 Современный вид таблицы Менделеева
Современный вид таблицы Менделеева
Размещение элементов в таблице удовлетворяет одновременно 2 условиям: они
️ организованы веса атомов,
️ химические и физические свойства каждого элемента сходны с предыдущим.
Закон справедлив для всех существующих и гипотетических элементов, исключая самых первых — они просто не имеют ничего перед собой (хотя многие пытаются разместить там гипотетический «эфир», ссылаясь на самого Менделеева, хотя он таких попыток не делал).
Интересно, что в первой версии было лишь 60 элементов таблицы. Сегодня их 118, а конечно число… Теоретически оно могло бы быть бесконечным, если бы не квантовая физика, но об этом чуть позже.
Закономерности изменения свойств элементов и их соединений в связи с положением в Периодической системе химических элементов Д.И. Менделеева
Напомним, что группами называют вертикальные ряды в периодической системе и химические свойства элементов главных и побочных подгрупп значительно различаются.
Свойства элементов в подгруппах закономерно изменяются сверху вниз:
- усиливаются металлические свойства и ослабевают неметаллические;
- возрастает атомный радиус;
- возрастает сила образованных элементом оснований и бескислородных кислот;
- электроотрицательность падает.
Все элементы, кроме гелия, неона и аргона, образуют кислородные соединения, существует всего восемь форм кислородных соединений. В периодической системе их часто изображают общими формулами, расположенными под каждой группой в порядке возрастания степени окисления элементов: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4, где символом R обозначают элемент данной группы. Формулы высших оксидов относятся ко всем элементам группы, кроме исключительных случаев, когда элементы не проявляют степени окисления, равной номеру группы (например, фтор).
Оксиды состава R2O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства.
Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения. Существуют четыре формы таких соединений. Их располагают под элементами главных подгрупп и изображают общими формулами в последовательности RH4, RH3, RH2, RH.
Соединения RH4 имеют нейтральный характер; RH3 — слабоосновный; RH2 — слабокислый; RH — сильнокислый характер.
Напомним, что периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
В пределах периода с увеличением порядкового номера элемента:
- электроотрицательность возрастает;
- металлические свойства убывают, неметаллические возрастают;
- атомный радиус падает.
Триады Деберейнера
Первая попытка систематизировать элементы была сделана еще в 1829 году немецким химиком Деберейнером. Он объединил некоторые элементы с общими свойствами в группы по три, назвав их триадами. Смысл этого закона заключался в том, что в каждой триаде масса среднего элемента была приблизительно равна среднему арифметическому между массами крайних элементов.
Такое представление было слишком далеко от совершенства, но уже являлось прообразом менделеевской системы. Проблема заключалась в ограничении групп всего тремя элементами, что подошло не для всех из них, даже известных на тот момент. Однако этот закон показал, что имеется какая-то связь между массами элементов и их химическими свойствами.
Основная разница — Менделеев против современной периодической таблицы
Периодическая таблица — это расположение химических элементов в соответствии с их химическими и физическими свойствами. Современная периодическая таблица была создана после серии различных версий периодической таблицы. Российский химик / профессор Дмитрий Менделеев первым предложил структуру периодической таблицы со столбцами и строками. Эта особенность является основным строительным блоком для современной периодической таблицы. Менделеев смог определить, что химические свойства элементов стали повторяться каждый раз после определенного количества элементов. Следовательно, термин «периоды» вошел в употребление, напоминая этот характер повторения. Столбцы в периодической таблице называются группы, и они группируют элементы с похожими свойствами. Строки в периодической таблице называются периоды, и они представляют собой наборы элементов, которые повторяются из-за обладания аналогичными свойствами. главное отличие между Менделеевым и современной периодической таблицей заключается в том, чтоПериодическая таблица Менделеева упорядочивает элементы на основе их атомной массы, тогда как Современная периодическая таблица упорядочивает элементы на основе их атомного номера.
Как понять таблицу Менделеева, если ты не шаришь?
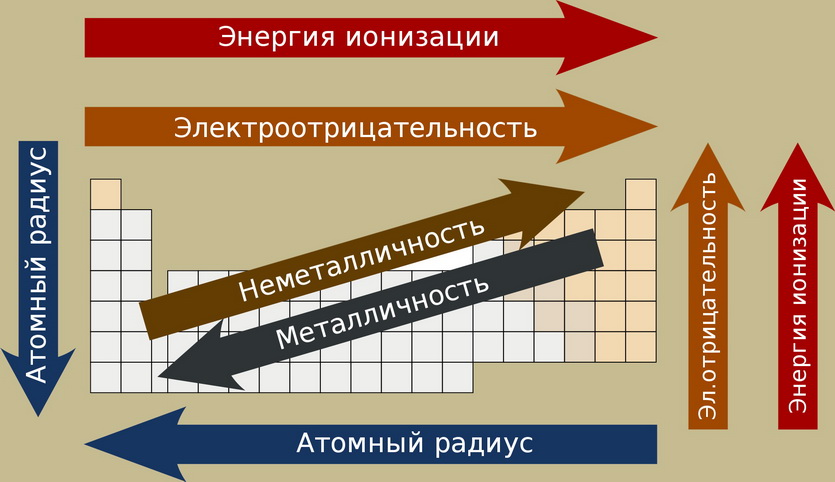 Краткая шпаргалка к Таблице Менделеева
Краткая шпаргалка к Таблице Менделеева
Периодический закон легко применять на практике. Ещё со школы мы все должны знать: натрий похож на калий, фтор похож на хлор, а золото — на серебро и медь. Следующий элемент просто как бы прибавляет к уже существующим ещё что-то.
По самой таблице так же можно узнать примерные свойства. В подгруппах сверху вниз:
️ усиливаются металлические свойства и ослабевают неметаллические (появляются свободные электроны — проводит ток);
️ возрастает атомный радиус (выше плотность/масса),
️ возрастает сила образованных элементом оснований и бескислородных кислот (действие сильнее),
️ электроотрицательность падает (хуже соединяется с другими элементами).
В периоде с увеличением порядкового номера элемента:
️ электроотрицательность возрастает (лучше образовывает соединения),
️ металлические свойства убывают, неметаллические возрастают (хуже проводит ток),
️ атомный радиус падает (хуже создает соединения).
Ещё одно свойство связано с традиционной, «короткой» формой таблицы, предложенной самим Менделеевым: если сложить её пополам, посредине IV группы, окажется, что элементы напротив друг друга могут образовывать соединения друг с другом.
Хотя на первый взгляд это не нужно в обыденности, таблица Менделеева помогает быстро понять, например: какая кислота «сильнее», что лучше проводит ток, к чему не стоит прикасаться, чем можно отравиться.






